电解质是什么检查项目(电解质有哪些种类)
- 网站运营杂谈
- 2024-08-14
- 267
首先定义: 化合物分为电解质和非电解质。在水溶液或熔融状态下能够导电的化合物叫电解质,在水溶液或熔融状态下不导电的化合物是非电解质。电解质分为强电...
首先定义:
化合物分为电解质和非电解质。在水溶液或熔融状态下能够导电的化合物叫电解质,在水溶液或熔融状态下不导电的化合物是非电解质。电解质分为强电解质和弱电解质,在水溶液或融融状态下几乎发生全部电离的电解质称为强电解质,强电解质不存在电离平衡,强电解质有强酸、强碱、活泼金属氧化物和大多数盐。在水溶液或熔融状态下发生部分电离的电解质称为弱电解质,弱电解质存在电离平衡,常见的弱电解质有弱酸、弱碱、少部分盐,还有水是弱电解质。
根据定义我们知道,不管是非电解质还是电解质,它肯定是化合物,而非混合物或者单质。非电解质是以共价键结合的化合物,除羧酸及其盐类、酚、胺等外,大多数有机化合物都是非电解质,如烃类、醇类、蔗糖、脂肪类、纤维素、淀粉、甘油等。还有就是一些常见的非金属氧化物,如一氧化碳、二氧化碳、二氧化硫、五氧化二磷,但是水是电解质,还有就是部分氢化物,如氨气、硫化氢、氯化氢等。

为什么电解质可以导电了?
电解质之所以在水溶液中能够导电,是因为电解质在水溶液中可以离解成离子,非电解质在水溶液中之所以不能导电是因为它在水溶液中不能离解成离子。物质在水溶液中能否导电是由其结构决定的。电解质包括离子型或强极性共价性化合物,非电解质包括弱极性或非极性共价型化合物。
非电解质:
在水溶液或熔融状态下都不导电的化合物。也就是在这两种情况下都不能电离生成自由移动的离子。
电解质:
在水溶液中或熔融状态下能导电的化合物。
① 电解质、非电解质的前提必须为化合物
故单质、混合物既不是电解质也不是非电解质
② 是否为电解质与其溶解度无必然联系
③ 电解质必须本身能电离出离子
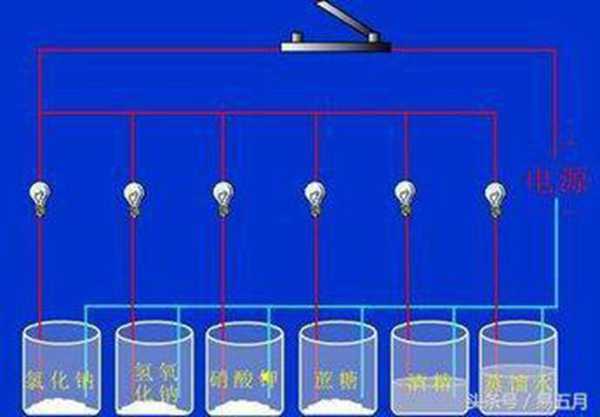
④ 电解质的导电:
导电的条件是溶于水或熔融状态
导电的本质是自由离子的定向移动
导电能力与离子浓度和离子所带电荷有关
⑤ 常见电解质:酸、碱、盐、水、活泼金属氧化物
常见非电解质:NH3、CO2、酒精、蔗糖等
在熔融和水溶液中都不能导电,以共价键结合,在水溶液中不发生电离反应的物质,称作非电解质。
这种物质一般是弱极性,或者非极性共价键化合物。